阿尔茨海默病(Alzheimer’s disease,AD)是最常见的神经退行性疾病,影响着全球约 5700 万人口。其典型病理特征为β-淀粉样蛋白(Aβ)在大脑中的异常沉积。这些沉积物被认为是驱动疾病发生发展的关键因素。近年来,靶向清除 Aβ 的疗法在临床试验中显示出延缓疾病进展的潜力。然而,现有策略,特别是抗体药物,常伴随严重副作用,如脑部炎症和出血(即淀粉样蛋白相关成像异常,ARIA)。因此,如何在高效清除致病蛋白的同时,最大限度地避免不良反应,成为 AD 治疗研发领域亟待突破的重大挑战。
针对这一难题,2026 年 3 月 4 日,北京干细胞与再生医学研究院/中国科学院动物研究所李伟研究员、胡宝洋研究员、周琪研究员联合团队在 Cell 杂志在线发表题为Efficient amyloid-β degradation in Alzheimer’s disease using SPYTACs 文章。该研究开发了一种能高效跨越血脑屏障(BBB)的新型靶向蛋白降解技术,名为可编程合成多肽介导的溶酶体靶向嵌合体(synthetic peptide-programmed lysosome-targeting chimeras,SPYTAC)。该技术实现了对外周和大脑中 Aβ 蛋白的协同清除,并在 AD 小鼠模型中验证了其显著的治疗效果和优越的安全性。

DOI:10.1016/j.cell.2026.01.034
SPYTAC 技术的核心在于其基于天然生理转运途径、高度模块化的全合成双特异性肽设计。研究团队巧妙选择了低密度脂蛋白受体相关蛋白1(LRP1)作为靶向受体。LRP1 是一种在血脑屏障和神经细胞表面高表达的受体,具有介导物质跨屏障转运和促进胞内降解的双重功能。通过将特异性结合 Aβ 的短肽与特异性结合 LRP1 的短肽进行模块化偶联,SPYTAC 可在细胞外“搭桥”,同时结合游离或聚集的 Aβ 蛋白与细胞膜上的 LRP1 受体,形成三元复合物。这一设计充分利用了 LRP1 的天然功能,既能引导 Aβ 进入细胞并被溶酶体降解,又能辅助 SPYTAC 携带 Aβ 穿越血脑屏障,实现外周与中枢 Aβ 的“双重清除”。在 5xFAD 阿尔茨海默病小鼠模型中,腹腔注射 SPYTAC 不仅有效降低了血浆和脑组织中的 Aβ 负荷,还能直接靶向已形成的老年斑,显著改善了小鼠的学习和记忆能力。
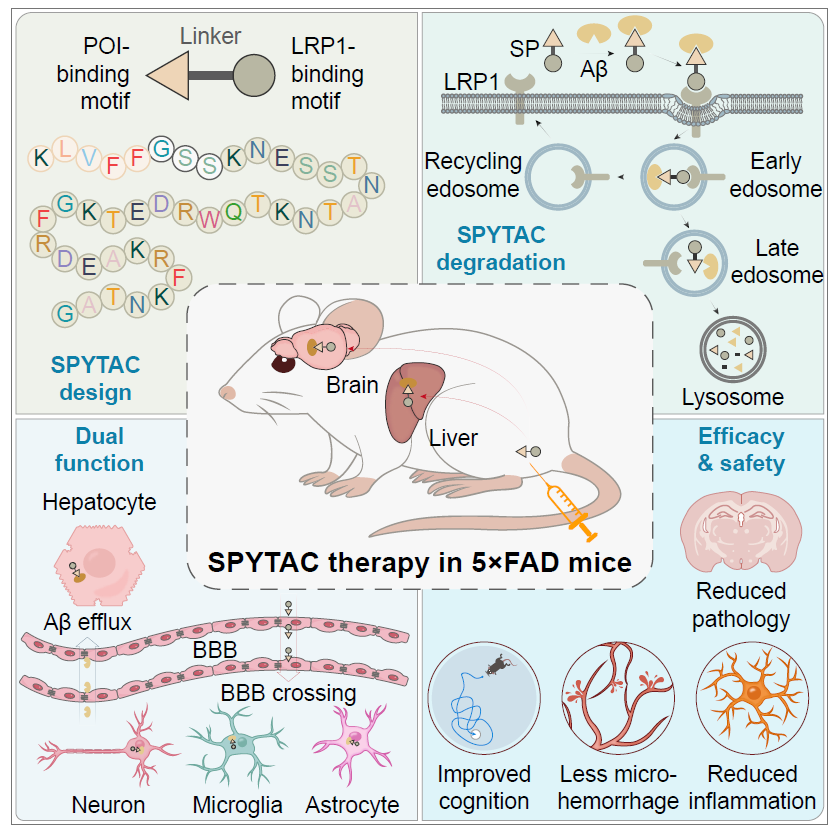
SPYTAC 有望实现阿尔兹海默病安全有效治疗
与传统的抗 Aβ 抗体药物相比,SPYTAC 技术不包含抗体的 Fc 片段,因此避免了免疫炎症反应和小胶质细胞过度活化,大幅降低了脑部炎症反应以及与脑淀粉样血管病相关的微出血风险,显示出更高的治疗安全性。
作为一种全合成的、可基因编码的模块化多肽平台,SPYTAC 在生产成本上具有成本低、周期短、易于规模化等优势。更重要的是,该平台具有良好的通用性,只需替换其中的目标结合肽模块,即可快速构建针对不同致病蛋白的降解剂,如 Tau 蛋白、PD-L1 蛋白,为多种神经退行性疾病乃至癌症的靶向治疗提供了通用且可编程的新型解决方案。
该研究突破了现有蛋白降解疗法在血脑屏障通透性和免疫安全性方面的瓶颈,不仅为阿尔茨海默病的治疗带来了全新的候选策略,也为精准靶向中枢神经系统疾病及其他由胞外致病蛋白驱动的疾病开辟了新路径。
此项研究由中国科学院动物研究所、中国科学院大学医学院等多家单位合作完成,得到了中国科学院战略先导专项和国家自然科学基金等项目资助。
【重要声明】以上内容仅用于知识科普,知识产权等所有权利归属于原作者,若有侵权,请联系esustain@163.com删除。