肿瘤细胞竟将毒性氨转化为“免疫燃料”!最新研究发现,肿瘤微环境中的氨(NH₃)并非单纯代谢废物,而是被调节性T细胞(Tregs)高效利用的“隐形武器”——肿瘤细胞通过释放氨毒害效应免疫细胞,而Tregs却借机激活代谢重编程,将氨转化为免疫抑制能量!
江苏省人民医院的研究团队通过空间多组学、单细胞测序等多维度分析,首次揭示这种“氨-Treg代谢适应”机制是肿瘤逃避免疫攻击的核心策略,更发现抗PD-1治疗后肿瘤死亡释放的氨会进一步强化Treg功能,成为免疫治疗耐药的“罪魁祸首”!
可借鉴的研究设计要点
《肿瘤产生的氨被调节性T细胞代谢,从而进一步抑制抗肿瘤免疫》
文献解读

01研究背景
肿瘤微环境(TME)中的代谢重编程是肿瘤免疫逃逸的关键因素。调节性T细胞(Tregs)在肿瘤组织中特异性富集并发挥强大的免疫抑制作用,但其在恶劣代谢环境中的适应机制尚不明确。
02研究目的
本研究聚焦于谷氨酰胺分解产物氨的代谢命运,揭示了Tregs通过独特的氨代谢通路实现生存优势并增强免疫抑制功能的完整机制。
03研究方法
1.空间多组学分析
对6例HCC患者组织进行空间转录组和空间代谢组整合分析,定位氨代谢区域与免疫细胞分布。
动物模型:建立HCC原位/皮下模型,结合免疫荧光和代谢组学验证氨-Treg关联。
2.体外功能实验
分离健康人或小鼠的Tregs、CD8+T、CD4+T细胞,用不同浓度NH₄Cl处理,检测增殖、凋亡、代谢。
基因操作:shRNA敲低ASL/SMS/PPARγ,CRISPR-Cas9构建突变体。
3.分子机制验证
转录调控:ChIP-qPCR验证FOXP3与SMS启动子结合, luciferase报告基因实验分析ASL/STAT3通路;
蛋白质相互作用:X射线晶体学解析精胺与PPARγ的结合结构,SPR、ITC测定亲和力;
代谢组学:LC-MS/MS追踪15N-NH₄Cl在尿素循环和多胺通路中的代谢流向。
4.体内治疗实验
小鼠模型:皮下/原位HCC模型,喂食氨饮食或注射抑制剂,联合抗PD-1治疗评估疗效;
临床样本:分析抗PD-1治疗前后患者肿瘤组织中氨浓度、Treg比例及代谢通路变化。
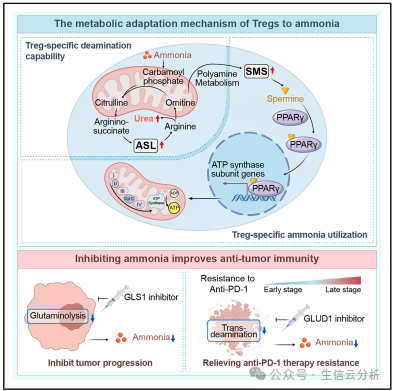
图解摘要
六步揭示“肿瘤氨代谢-Treg免疫抑制”因果轴
01空间定位
整合空间代谢组与转录组,发现Treg富集区呈现“高谷氨酰胺分解-低尿素循环”的代谢异质性特征。
02功能验证
通过体外氨处理及动物模型,证实氨选择性增强Treg存活并抑制效应T细胞。
03分子挖掘
利用单细胞测序与同位素标记,揭示Treg通过SRC3-STAT3轴上调ASL激活尿素循环解毒。
04通路拓展
发现FOXP3转录调控SMS,驱动精胺合成并激活PPARγ线粒体功能轴。
05靶点确认
结合X射线晶体学与亲和质谱,精确定位精胺-PPARγ直接互作界面及关键残基。
06临床关联
通过PD-1治疗队列分析,验证肿瘤细胞死亡通过转脱氨作用加剧氨积累,驱动免疫治疗耐药。
主要结果
肿瘤“氨工厂”的区位优势——Tregs的富集地图
研究团队首先利用空间转录组与代谢组学技术,绘制了人类肝细胞癌(HCC)的代谢地图。他们发现,肿瘤内部存在代谢异质性区域:某些区域谷氨酰胺分解(glutaminolysis)异常活跃,导致氨含量升高,而这里正是Tregs频繁出没的“热点”。相反,CD8+和CD4+效应T细胞在这些区域却纷纷凋亡。【图1A-D】。
进一步分析显示,只有同时具备“高谷氨酰胺分解+低尿素循环活性”的区域,Tregs才显著富集【图1D-E】。尿素循环本是肝脏解毒氨的主要途径,但在肿瘤中,它的活性降低导致氨堆积,意外地为Tregs创造了生存优势【图1G-H】。
这一发现不仅解释了Tregs在肿瘤中的空间分布偏好,还突出了氨代谢平衡在免疫调控中的核心作用,提示氨代谢失衡是驱动免疫抑制的核心起点【图1k-l】。
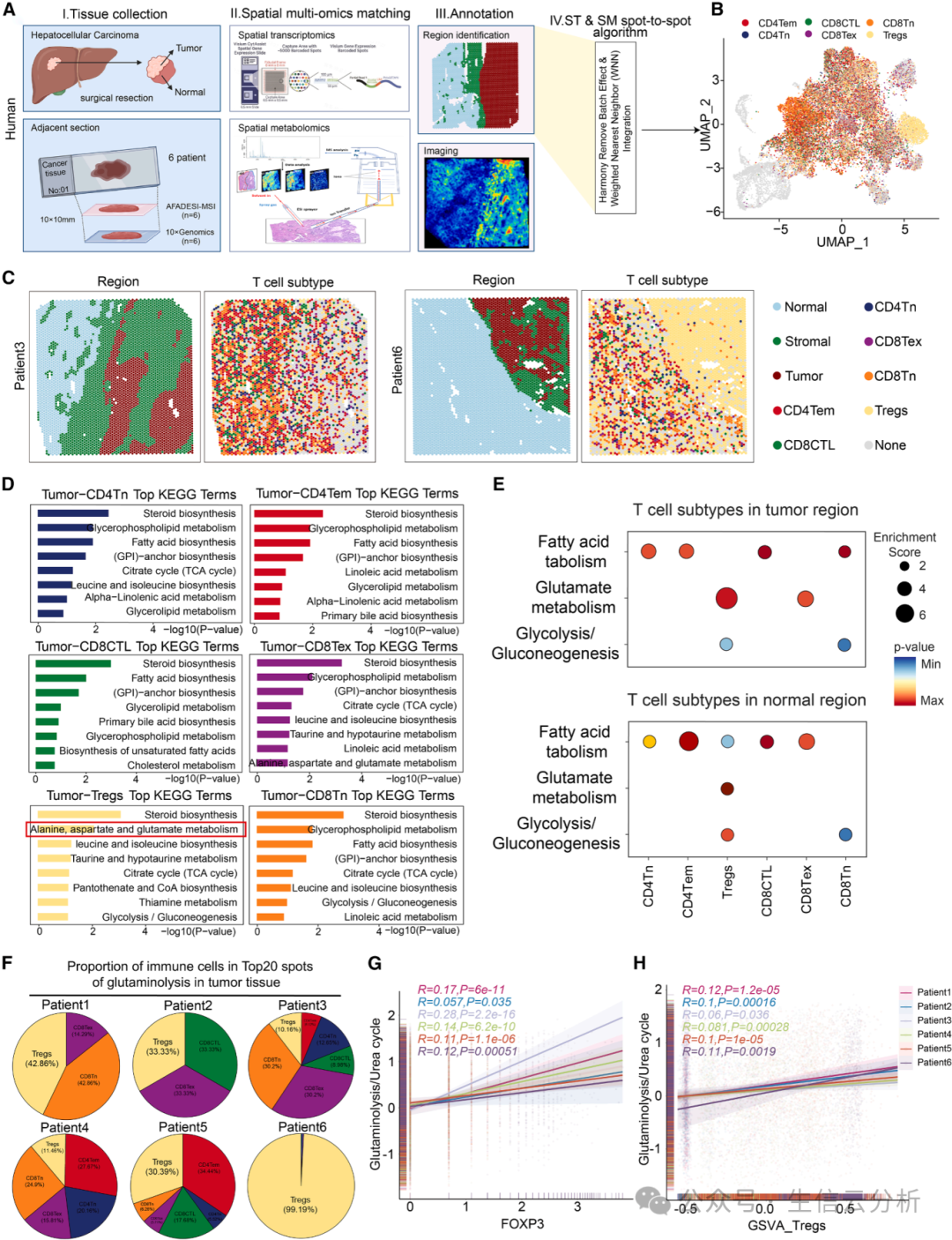
图1.高谷氨酰胺分解与低尿素循环活性是肿瘤亚区Treg富集的关键代谢特征
02Tregs的“氨抗性”
氨对大多数细胞是有毒的,但Tregs却展现了惊人的韧性。团队在体外用不同浓度氨处理T细胞,发现低浓度氨(5mM,模拟肿瘤水平)反而增强Tregs的增殖和功能(如上调FOXP3、PD-1和CTLA-4),而CD8+和CD4+ T细胞则大量凋亡【图2A-C】。
在活体实验中,给小鼠喂食氨富集饮食后,Tregs在脾脏和血液中数量飙升,其他T细胞则被抑制【图2F-I】。
这表明,氨像一把“双刃剑”——对效应T细胞是毒药,对Tregs却是“补品”。这种选择性优势解释了为何肿瘤中Tregs能逆势增长,而免疫反应被压制【图2J】。
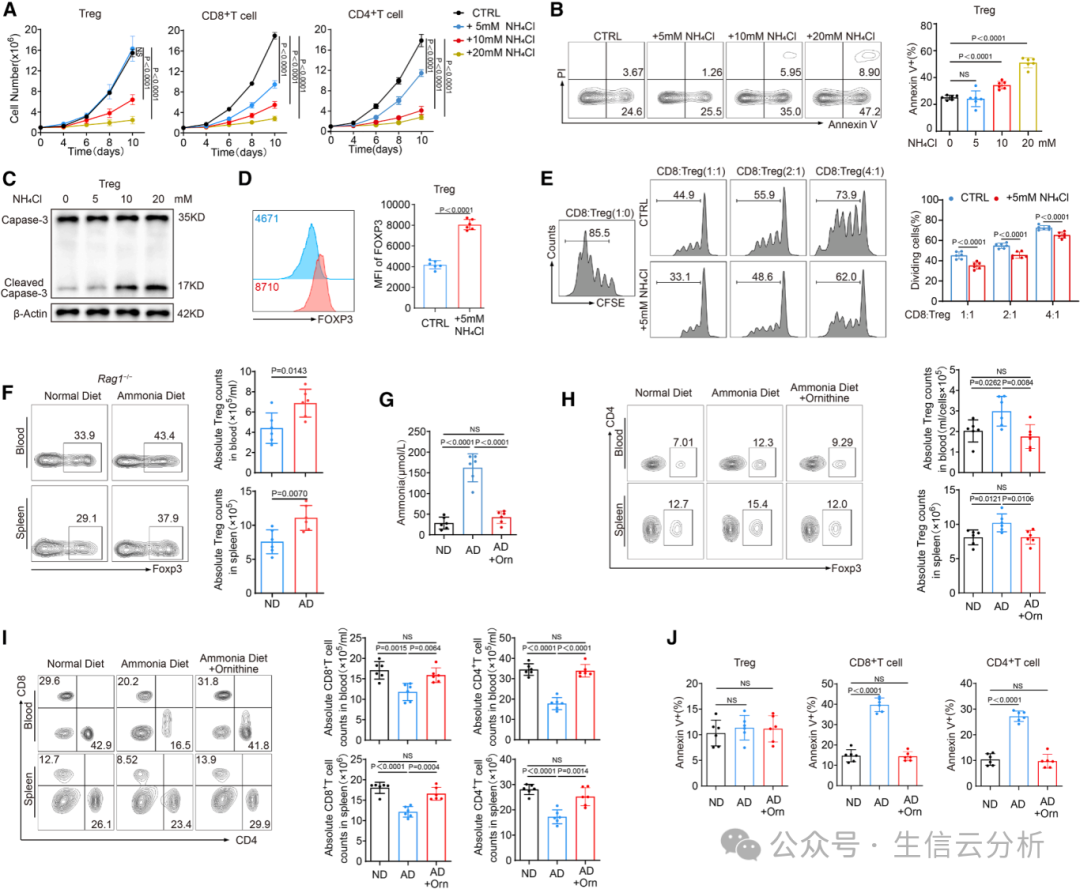
图2.调节性T细胞(Tregs)而非CD8+或CD4+T细胞可抵抗氨诱导的细胞凋亡
03Tregs的解毒妙招
Tregs为何能耐受氨?团队发现,它们拥有高效的“解毒系统”——尿素循环。从人HCC样本分离的Tregs显示更低的细胞内氨水平和更高的尿素循环中间产物【图3A-B】。
机制上,氨暴露会特异性上调Tregs中的精氨基琥珀酸裂解酶(ASL),这是尿素循环的关键酶。通过基因敲低实验,证明ASL是Tregs解毒氨的“关键开关”:一旦ASL被抑制,Tregs就会积累氨、走向凋亡【图3C-E】。
氨处理能上调Tregs中ASL的mRNA和蛋白水平,而CD8+ T细胞无此反应【图3f-h】。敲低ASL后,Tregs内氨积累增加,凋亡率上升,且尿素循环代谢紊乱【图3i-n】。
小鼠模型中也证实,ASL缺陷的Tregs在氨环境中失去保护优势,肿瘤生长减缓【图3l-m】。这项工作明确了ASL是Tregs响应氨信号的核心分子,尿素循环是其解毒氨的重要途径。
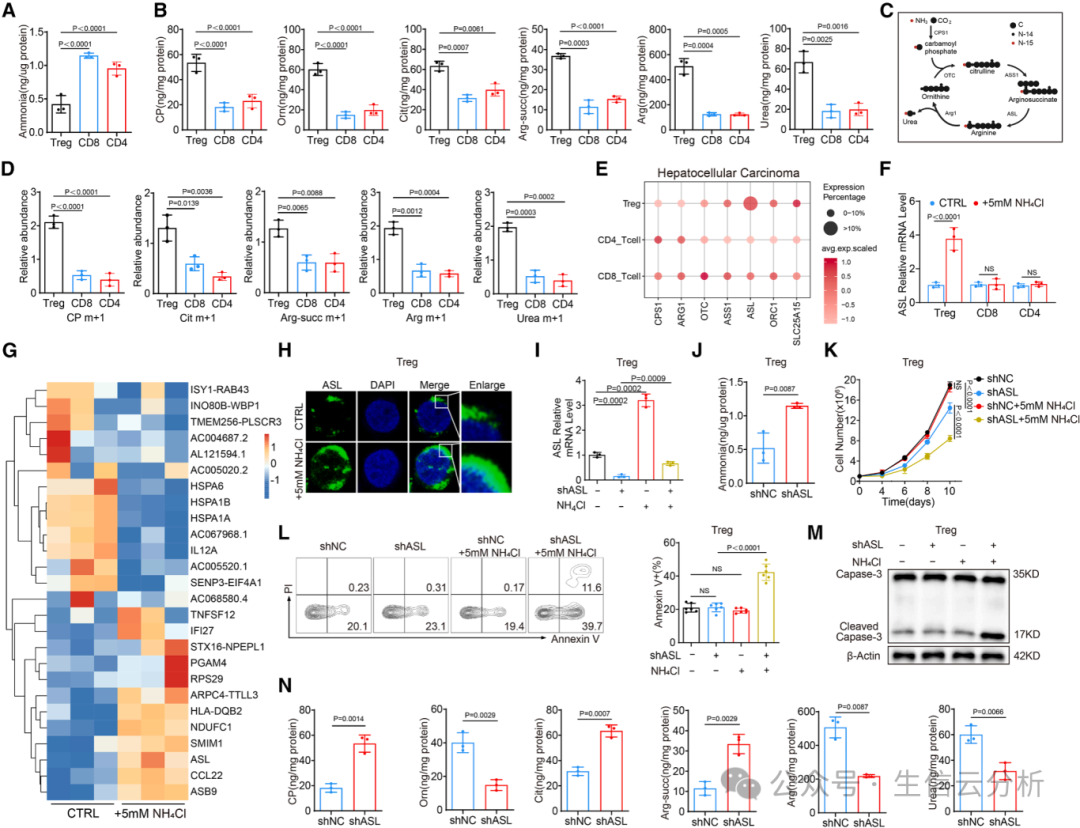
图3.氨暴露通过上调精氨酸琥珀酸裂解酶表达诱导调节性T细胞(Tregs)中尿素循环的激活
04氨的“变废为宝”
解毒只是第一步,Tregs还能将氨“废物利用”。团队发现,氨处理后的Tregs氧化磷酸化(OXPHOS)显著增强——这是细胞能量的“涡轮增压”【图4A-B】。
究其原因,氨通过Tregs特有的转录因子FOXP3上调精胺合成酶(SMS),后者将尿素循环的副产品鸟氨酸转化为精胺【图4C-I】。
敲低SMS后,氨诱导的OXPHOS增强和免疫抑制功能被废除【图4j-n】。启动子分析结合染色质免疫沉淀实验证明,FOXP3直接结合SMS启动子区域,驱动其表达【图4o-v】。
这揭示了Tregs的“代谢智慧”:它们不仅解毒氨,还将其转化为促进自身能量的分子,从而在肿瘤中保持活跃。
图4.氨通过FOXP3驱动的SMS表达促进调节性T细胞(Tregs)的 OXPHOS
05精胺的“能量钥匙”:靶向PPARγ,激活线粒体
精胺如何增强OXPHOS?团队通过亲和蛋白质组学发现,精胺直接结合转录因子PPARγ——一个调控代谢的关键蛋白【图5A】。
实验显示,外源精胺无法进入细胞,但内源产生的精胺(通过SMS)能稳定PPARγ,进而上调多个线粒体复合物基因(如NDUFC1、SDHC等)【图5B-F】。
通过亲和蛋白质组学,他们发现精胺直接结合转录因子PPARγ【图5G-K】。敲低PPARγ后,氨诱导的OXPHOS增强消失【图5P】。小鼠模型中,PPARγ缺陷的Tregs在氨环境中无法提升免疫抑制功能。
这一环节揭示了精胺-PPARγ轴是连接氨代谢与Tregs功能增强的桥梁。

图5.亚精胺通过PPARγ增强调节性T细胞(Treg)OXPHOS 及免疫抑制能力
06精胺与PPARγ的“分子握手”:结构层面的确证
为验证结合机制,团队运用结构生物学手段(如X射线晶体学),发现精胺通过静电作用和氢键与PPARγ的Glu319、Ser370和Glu371残基直接互动【图6A-H】。
突变这些位点后,结合能力丧失,Tregs的OXPHOS也无法被氨增强。这就像找到了精胺作用的“精确锁孔”,从原子层面揭示了Tregs代谢重编程的根源【图6I-N】。
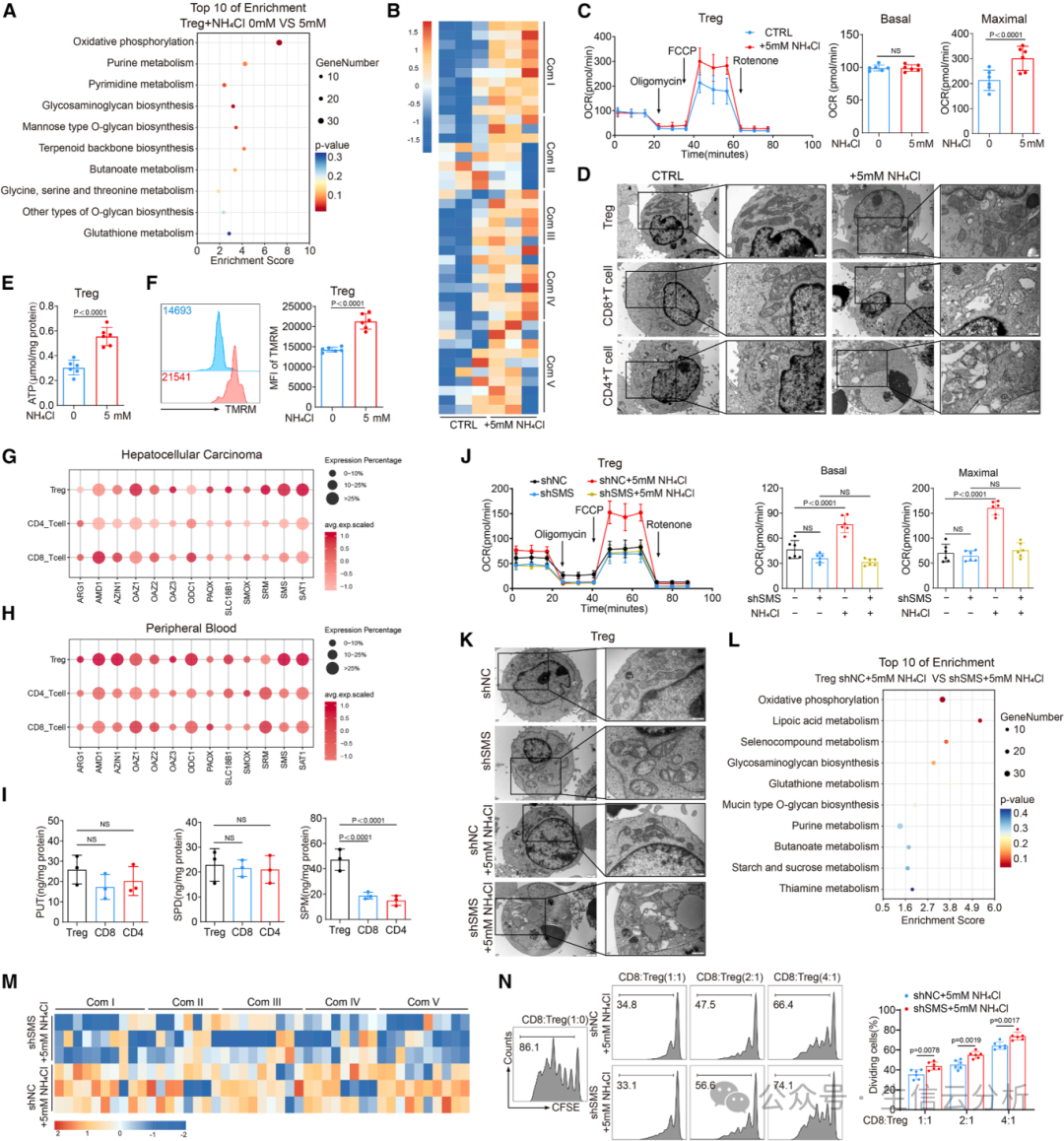
图6.精胺直接结合PPARγ并调控调节性T细胞(Tregs)中线粒体复合物的形成与OXPHOS
07免疫治疗的“反弹陷阱”:抗PD-1疗法意外加剧氨释放
最后,团队将目光投向临床:为何抗PD-1治疗常出现抵抗?分析接受抗PD-1治疗的HCC患者样本,发现治疗后肿瘤组织氨水平升高,Tregs浸润增加【图7a】。
他们发现,PD-1抗体诱导肿瘤细胞死亡时,会通过“转脱氨作用”(transdeamination)大量释放氨,而非传统的谷氨酰胺分解。这反而强化了Tregs的功能,形成恶性循环【图7B-H】。
在小鼠模型中,联合使用谷氨酸脱氢酶(GLUD)抑制剂(阻断转脱氨)能有效降低氨水平,逆转Tregs介导的抵抗【图7E-N】。
这警示我们,免疫治疗可能无意中“喂饱”了Tregs,而靶向氨生产(如GLUD抑制剂)或许是破局关键。
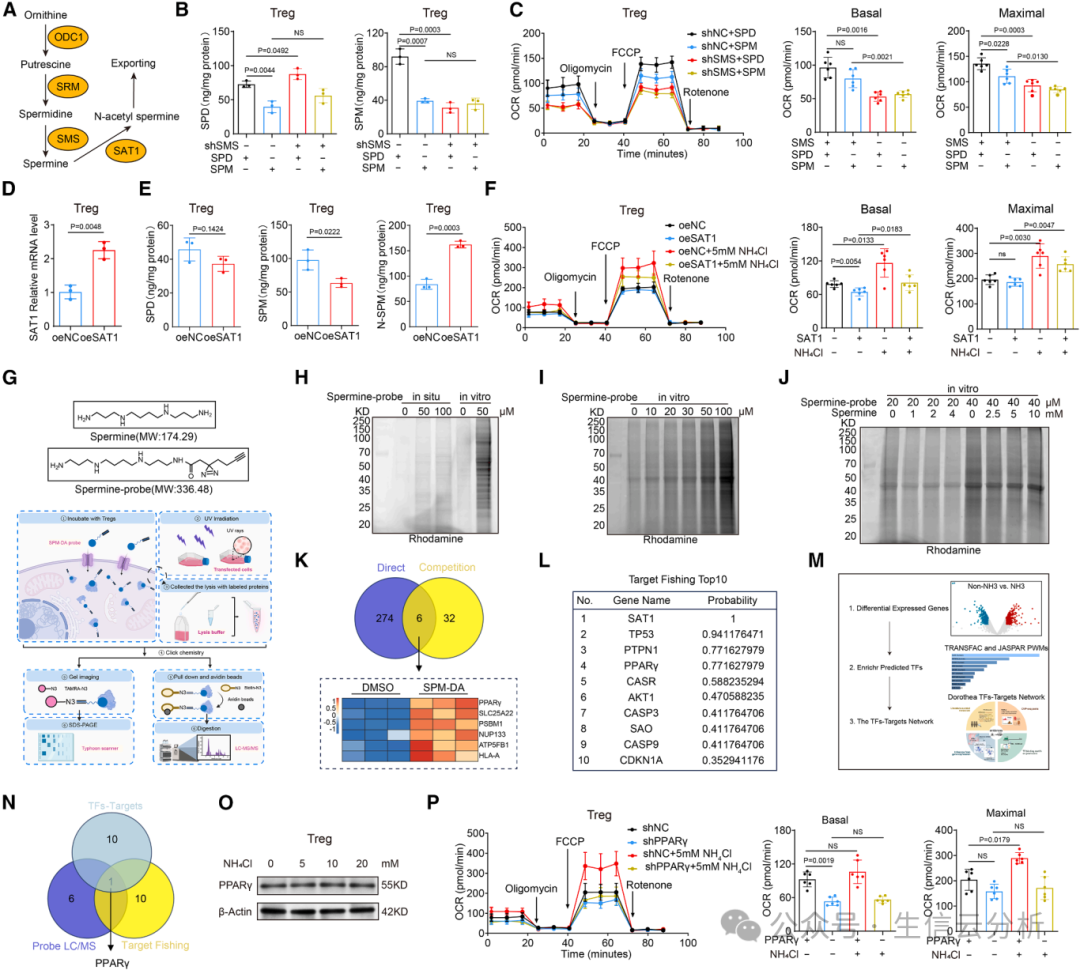
图7.抗PD-1疗法诱导的细胞死亡产生的氨可增强调节性T细胞(Tregs)并导致免疫治疗耐药性
研究意义与创新点
方法创新:首次应用空间多组学解析TME代谢异质性与免疫细胞分布的关联。
机制深度:从代谢物感知到表观遗传调控,阐明了完整的信号通路。
转化价值:提出靶向氨代谢克服免疫治疗耐药的新策略。
临床意义:免疫治疗引发的肿瘤细胞死亡会加剧氨累积,是导致耐药的新原因。
文章小结
本文通过空间多组学、分子生物学和体内外实验,系统阐明了肿瘤氨代谢如何驱动Tregs富集和功能增强,并揭示了抗PD-1耐药的新机制。该研究为肿瘤免疫治疗提供了代谢干预的新方向,有望通过靶向氨生成或Tregs的氨适应通路,克服免疫耐药,提高疗效。
【重要声明】以上内容仅用于知识科普,知识产权等所有权利归属于原作者,若有侵权,请联系esustain@163.com删除。
来源:https://doi.org/10.1016/j.cell.2025.11.034