你肠道里的Trp-CA竟通过孤儿受体MRGPRE悄悄调节血糖!最新研究发现,肠道微生物产生的色氨酸-胆酸(Trp-CA)通过激活肠道孤儿GPCR受体MRGPRE,双通路促进GLP-1分泌,改善高脂饮食小鼠血糖稳态。
北京大学姜长涛教授团队研究团队通过临床队列关联、动物模型验证、结构生物学解析和微生物溯源,揭示了Trp-CA-MRGPRE-GLP-1新代谢调控通路,为2型糖尿病治疗提供新靶点!
文献解读

01研究背景
2型糖尿病(T2D)是一种全球性代谢疾病,常伴随肥胖和心血管问题。肠道微生物群及其代谢物(如胆汁酸)在宿主葡萄糖稳态中扮演重要角色。传统胆汁酸通过FXR和TGR5受体调节代谢,但新发现的微生物氨基酸结合胆汁酸(MABAs)的生理功能尚不明确。
02研究目的
本研究聚焦于微生物氨基酸偶联胆汁酸(MABAs) 的生理功能,首次发现色氨酸-胆酸(Trp-CA) 在2型糖尿病(T2D)患者中显著降低,并通过激活孤儿GPCR受体MRGPRE促进GLP-1分泌,从而改善葡萄糖稳态。
03研究方法
1.数据来源:
人类样本:
招募了80名个体(40名新诊断的2型糖尿病(T2D)患者和40名健康对照),收集粪便样本进行非靶向代谢组学分析。
另一独立队列(49名个体,包括21名健康对照和28名T2D患者)用于验证Trp-CA与GLP-1水平的相关性。
动物模型:使用C57BL/6J小鼠、Mrgpre基因敲除(Mrgpre⁻/⁻)小鼠、肠道特异性Mrgpre敲除(Mrgpre^ΔIE)小鼠、以及Arrb1⁻/⁻、Arrb2⁻/⁻等基因修饰小鼠。小鼠饲喂高脂饮食(HFD)诱导T2D模型。
细菌菌株:筛选98种肠道细菌(从人类粪便分离),重点研究双歧杆菌(Bifidobacterium)的胆汁酸代谢功能。
2.验证实验:
细胞实验:包括人胚胎肾细胞(HEK293T)、小鼠肠内分泌L细胞系(GLUTag、STC-1)和人肠内分泌L细胞系(NCI-H716),用于受体筛选和信号通路研究。
人类关联性研究:通过LC-MS/MS代谢组学比较T2D患者与健康对照的粪便微生物氨基酸共轭胆汁酸(MABAs)水平,发现Trp-CA是差异最显著的代谢物。
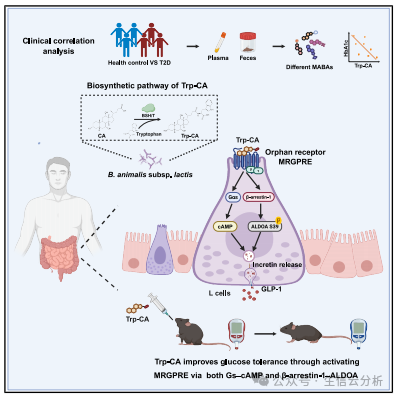
图解摘要
六步构建“微生物胆汁酸-葡萄糖稳态”因果桥梁
01临床关联挖掘
基于80人队列的代谢组学分析,发现Trp-CA在T2D患者粪便中显著降低,且与空腹血糖、HbA1c等临床指标呈负相关。
02动物功能验证
在高脂饮食诱导的糖尿病小鼠中,口服Trp-CA可快速改善葡萄糖耐受性,且效应独立于肥胖发生。
03受体靶点锁定
通过GPCR组筛选技术,首次鉴定孤儿受体MRGPRE为Trp-CA的特异性激活靶点,基因敲除实验证实其必要性。
04下游信号解析
揭示Trp-CA通过MRGPRE激活Gs-cAMP和β-arrestin-1-ALDOA双通路,协同促进GLP-1分泌。
05结构基础探索
结合分子对接与突变验证,阐明Trp-CA与MRGPRE的氢键网络和疏水相互作用,关键残基决定结合特异性。
06微生物源追溯
筛选98种肠道细菌,发现双歧杆菌的胆汁盐水解酶/转移酶负责Trp-CA合成,工程菌定植重现代谢益处。
主要结果
Trp-CA与T2D的临床关联
研究团队首先从临床入手,招募了80名参与者(40名T2D患者和40名健康对照),通过非靶向代谢组学分析粪便样本。
结果发现,T2D患者的粪便代谢谱与健康人群存在显著差异,而其中Trp-CA的水平下降最为明显——它在糖尿病患者中大幅降低,且与空腹血糖、糖化血红蛋白等指标呈负相关【图1A-G】。
Trp-CA的减少可能暗示了其在血糖调控中的重要作用。
更有趣的是,Trp-CA虽然只占胆汁酸池的极小部分,但其稳定性与已报道的胆汁酸相当,且在抗生素处理或无菌小鼠粪便中几乎检测不到,说明它的产生依赖肠道微生物。团队进一步合成Trp-CA并验证其结构,为后续机制研究打下基础。
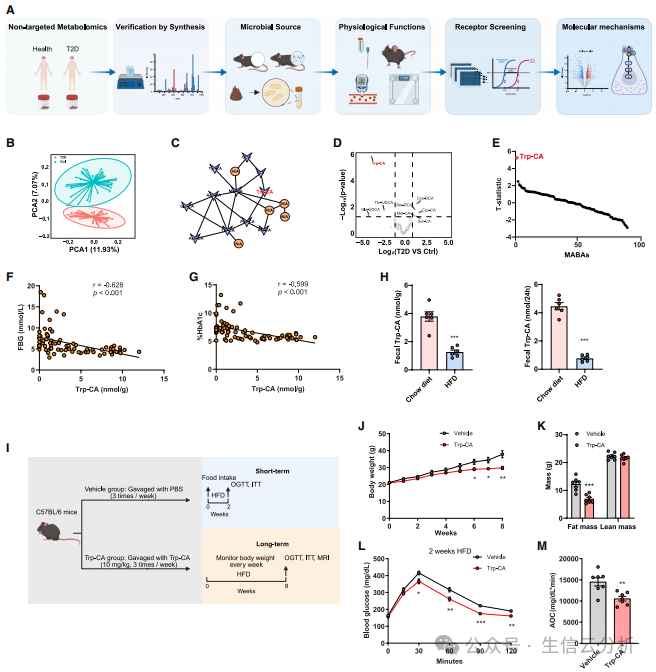
图1.Trp-CA缓解 HFD 诱导的葡萄糖不耐受
为了验证Trp-CA的功能,研究团队给高脂饮食(HFD)诱导的糖尿病小鼠灌服Trp-CA。
结果令人振奋:Trp-CA处理的小鼠体重增加更少、脂肪量下降,且葡萄糖耐受性显著改善【图1H-M】。这种效应在肥胖发生前就已出现,提示Trp-CA可能独立于减肥作用直接调控血糖。
更关键的是,在已肥胖的小鼠中,Trp-CA同样能逆转葡萄糖不耐受,就像一把“代谢钥匙”开启了改善之门。
02锁定孤儿受体MRGPRE:Trp-CA的“专属开关”
Trp-CA如何发挥作用?团队没有止步于已知胆汁酸受体(如TGR5或FXR),而是通过GPCR筛选系统,发现Trp-CA能特异性激活孤儿受体MRGPRE——一个属于瘙痒受体家族但未被报道参与瘙痒的蛋白【图2A-C】。
通过荧光能量共振转移(FIAsH-BRET)实验,他们观察到Trp-CA结合后引起MRGPRE胞外构象变化。
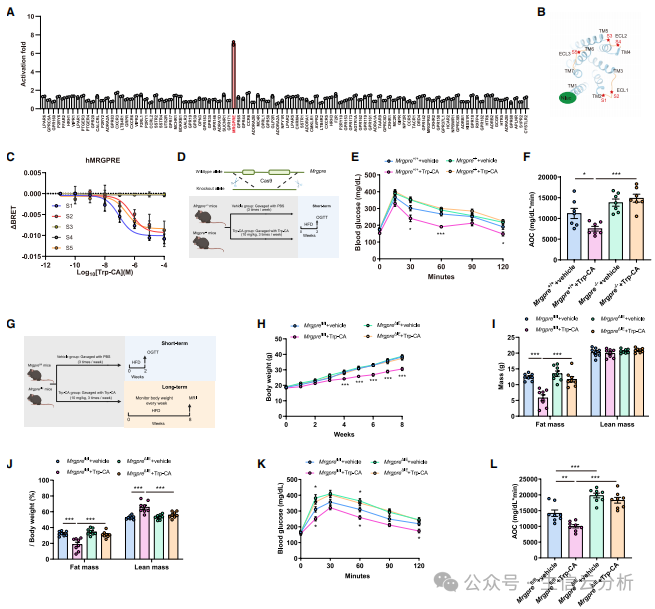
图2.Trp-CA是孤儿受体 MRGPRE 的内源性配体
基因敲除实验更是铁证如山:在全身或肠道特异性敲除Mrgpre的小鼠中,Trp-CA的益处完全消失【图2D-L】。这表明MRGPRE是Trp-CA发挥作用不可或缺的媒介,破解了多年来该受体生理功能的谜团。
03GLP-1分泌的幕后推手:Trp-CA-MRGPRE轴心作用
既然Trp-CA主要作用于肠道,团队顺藤摸瓜,发现它能刺激肠内分泌L细胞分泌胰高血糖素样肽-1(GLP-1)——一种著名的“降糖激素”【图3A-D】。
在细胞实验中,Trp-CA直接促进GLP-1分泌,且这一效应被MRGPRE敲低所阻断。更妙的是,MRGPRE在L细胞中高表达,且Trp-CA处理后可引发受体内化,就像激素与受体“拥抱”后一起进入细胞内部。
这就像在珍贵的画作前放置了一个更容易着火的屏障,火苗会先烧掉屏障,从而保全画作。
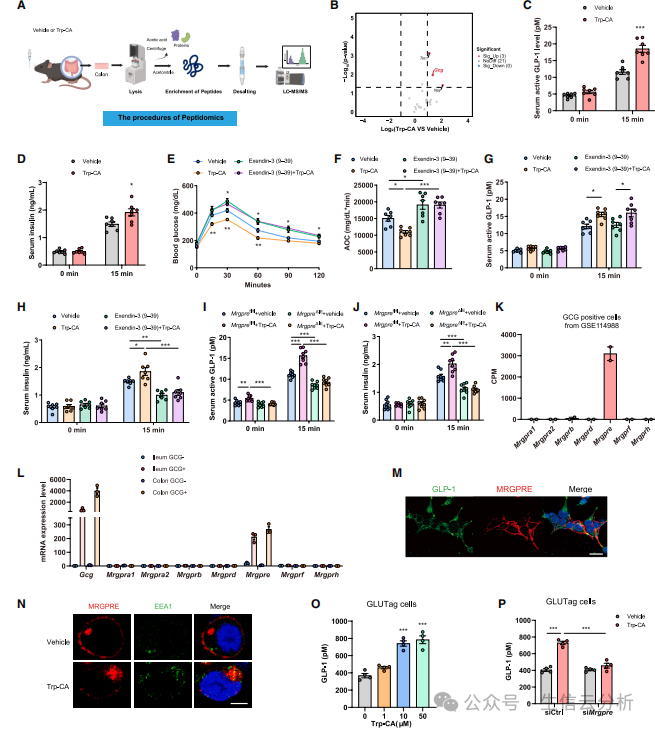
图3.Trp-CA通过促进 GLP -1分泌改善葡萄糖耐量
04结构生物学揭秘:Trp-CA如何精准激活MRGPRE
为了看清Trp-CA与MRGPRE的“分子之舞”,团队尝试解析复合物结构。虽因聚集问题未能获得人源MRGPRE的高分辨率结构,但他们通过同源蛋白(如马源MRGPRE)和分子动力学模拟,揭示了结合模式【图4A-I】。
Trp-CA的固醇核心嵌入受体口袋,其3个羟基与关键氨基酸形成氢键,而色氨酸部分则通过疏水作用稳定结合。
点突变实验证实,这些相互作用是激活MRGPRE所必需的。
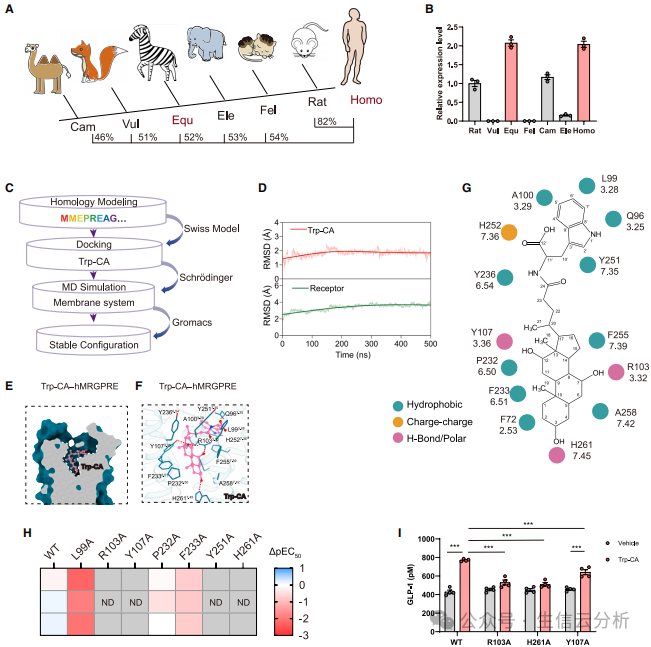
图4.Trp-CA与hMRGPRE结合及激活的结构基础
05疾病另一面:提升7-DHC水平,保护脏器损伤
深入机制探索揭示,Trp-CCA激活MRGPRE后,会启动两条平行的信号通路来促进GLP-1分泌:
经典通路:通过Gαs蛋白激活cAMP信号通路。
创新通路:通过招募β-arrestin-1蛋白,进一步与一种代谢酶(ALDOA,醛缩酶A)结合,并促进其磷酸化,从而增强L细胞的糖酵解效率,快速产生更多能量(ATP),驱动GLP-1的分泌【图5H-K】。
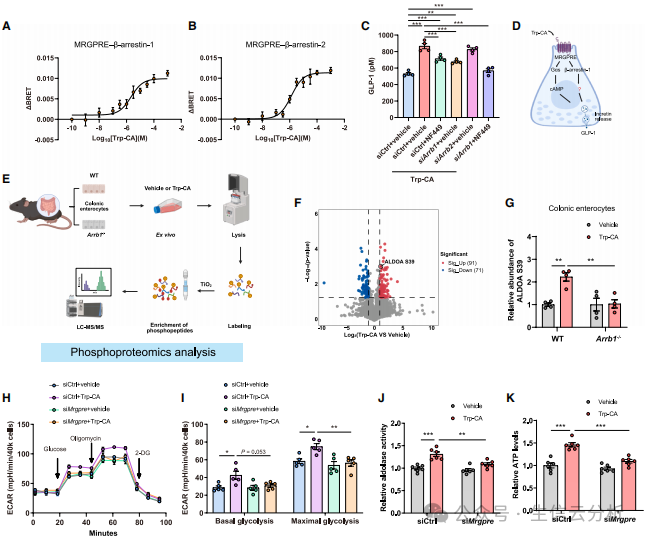
图5.Trp-CA通过诱导ALDOA磷酸化促进细胞糖酵解
06Trp-CA通过MRGPRE促进GLP-1分泌
如果把这第二条通路比作一个加速器,那么磷酸化的ALDOA就像是给细胞代谢踩下了油门。当研究人员在细胞和动物模型中抑制ALDOA时,Trp-CA的提升糖酵解和促进GLP-1分泌的作用就被显著削弱了【图6G, H】。
这条新发现的MRGPRE-β-arrestin-1-ALDOA通路,是本研究最精彩的机制发现之一。
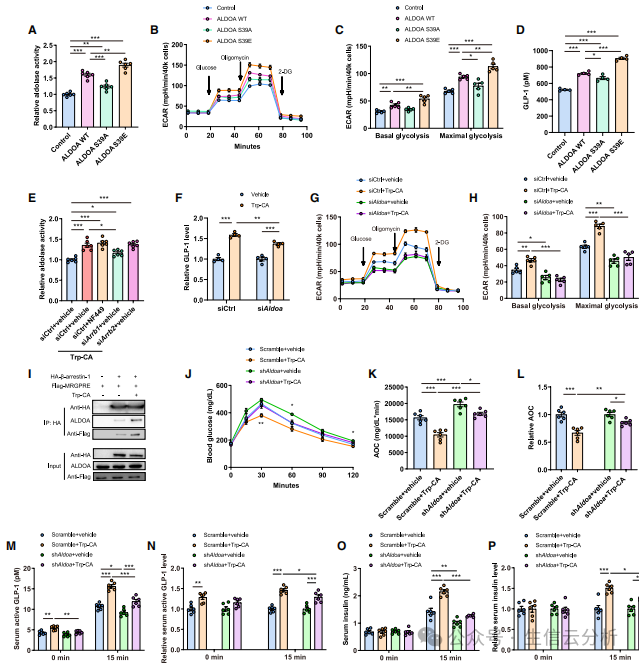
图6.Trp-CA通过MRGPRE-β-arrestin-1-ALDOA途径部分诱导GLP -1分泌
07微生物工厂:双歧杆菌负责生产Trp-CA
最后,团队追踪Trp-CA的源头,筛选了98种肠道细菌,发现双歧杆菌(尤其是B. animalis subsp. lactis)能高效合成Trp-CA【图7A-C】。
其背后的“工匠”是细菌胆汁盐水解酶/转移酶(BSH/T),该酶能催化色氨酸与胆酸结合。将表达BSH/T的工程菌定植于小鼠肠道后,葡萄糖耐受性改善,GLP-1水平上升,且该效应依赖MRGPRE【图7D-J】。这就像发现了一个“微生物制药厂”,为益生菌疗法提供了新思路。
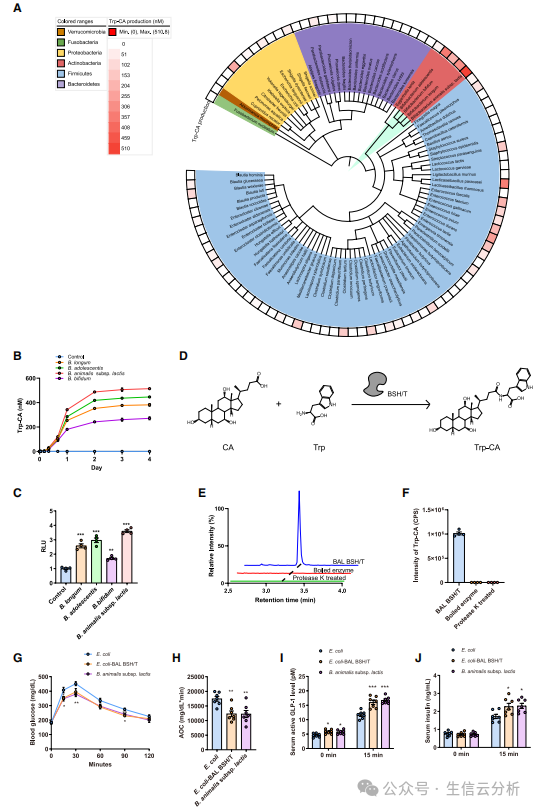
图7.B. animalis subsp. lactis的BSH/T负责色氨酸羧化酶(Trp-CA)的合成
研究意义与创新点
方法创新:MRGPRE作为一个新的胆汁酸受体和糖尿病治疗潜在靶点横空出世。
机制突破:发现了β-arrestin-1调控细胞代谢酶ALDOA从而影响激素分泌的新通路。
转化价值:Trp-CA口服吸收差,主要作用于肠道,可能避免传统胆汁酸药物(如OCA)的全身性副作用;MRGPRE成为T2D治疗的新靶点,为开发肠道局部作用药物提供方向。
文章小结
这项研究从临床现象出发,通过多维度实验揭示了Trp-CA-MRGPRE轴在血糖调控中的核心作用,不仅填补了微生物胆汁酸生理功能的空白,还为糖尿病治疗提供了新靶点。相比现有胆汁酸药物(如奥贝胆酸)易引起瘙痒的缺点,Trp-CA因口服吸收差而可能避免外周副作用,更具应用潜力。未来,调控肠道菌群或开发MRGPRE激动剂有望成为糖尿病管理的新策略。
【重要声明】以上内容仅用于知识科普,知识产权等所有权利归属于原作者,若有侵权,请联系esustain@163.com删除。
来源:DOI:10.1016/j.cell.2025.05.010