当一篇论文同时满足三个条件—登上 Cell、作者来自微软、提出“虚拟免疫人群”这一概念,它已经不只是一项技术工作,而是一条值得被认真解读的信号。

这篇 Cell 论文真正重要的,不是“AI 又预测了什么”,而是肿瘤免疫研究拥有了“人群级”的研究对象。
问题从一开始就不是“模型不够好”肿瘤免疫微环境(Tumor Immune Microenvironment, TIME)被认为是:决定肿瘤进展的关键因素、影响免疫治疗疗效的核心变量、新一代生物标志物的重要来源。
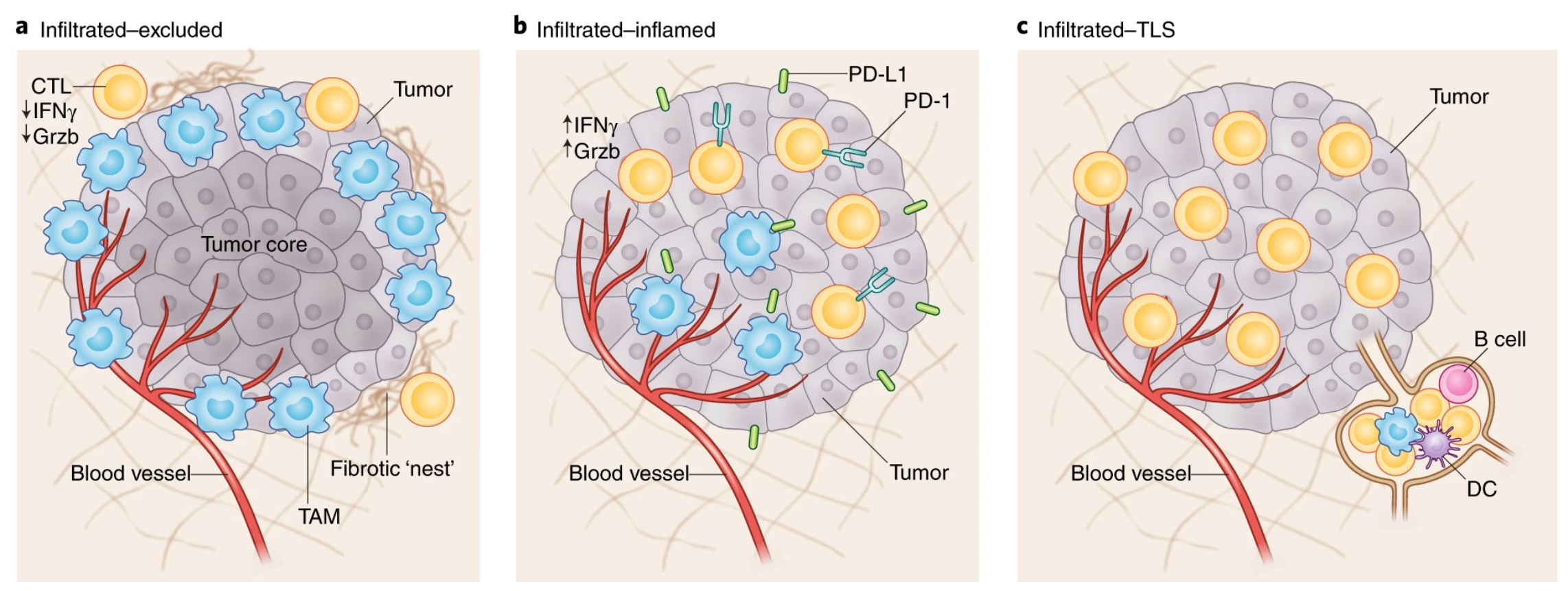
但现实是,真正能解析 TIME 的空间蛋白技术(mIF、CODEX、IMC)始终无法规模化,成本高、通量低、难以进入真实世界大队列,结果就是一个长期存在的结构性矛盾:我们对免疫机制的理解越来越精细,但这些理解几乎全部来自“小样本世界”。
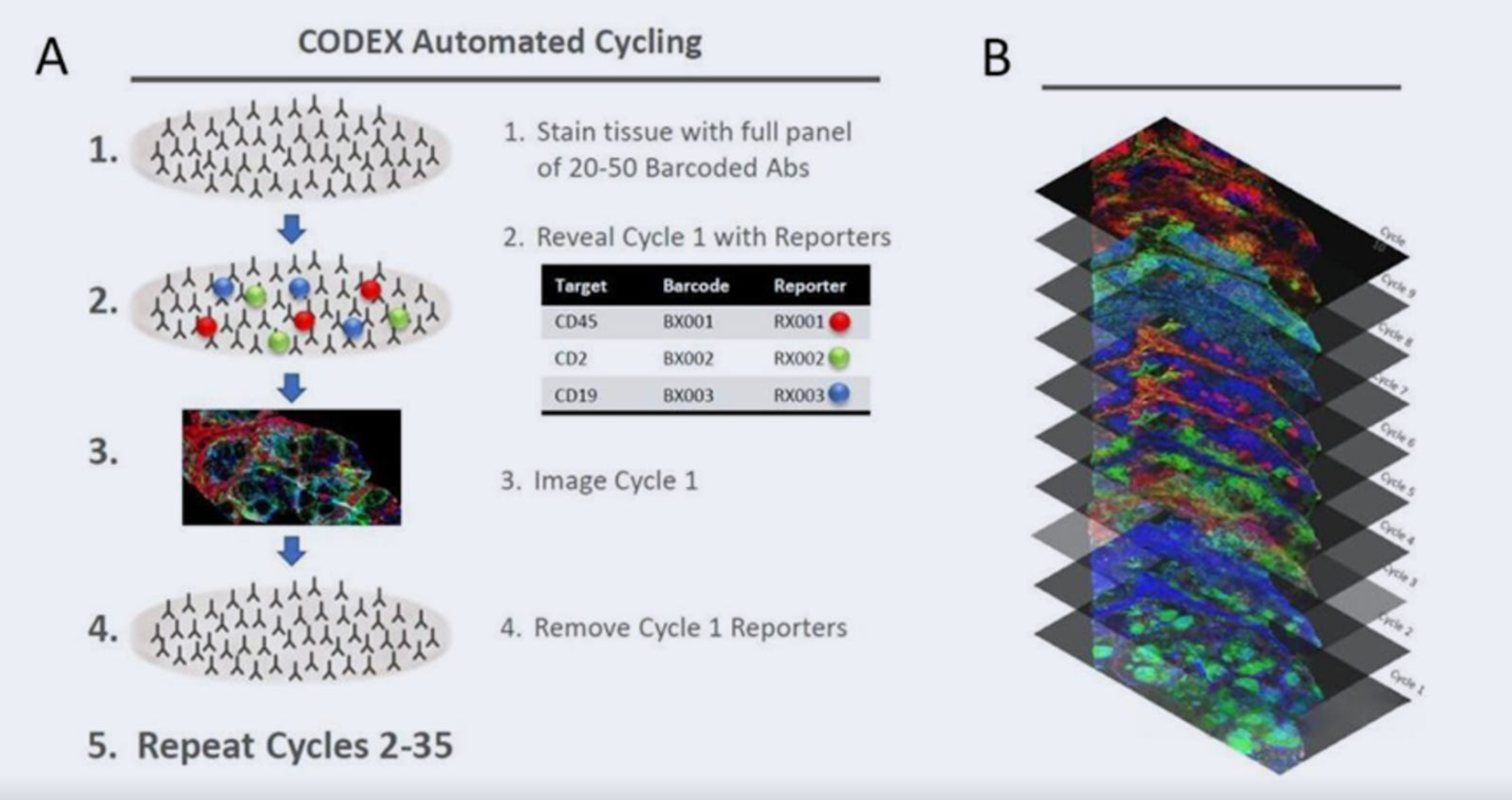
微软的切入点:不是新实验,而是“补全可观测性”微软团队并没有试图发明新的免疫实验,而是提出了一个更现实的问题:既然 H&E 切片在几乎所有患者中都存在,而免疫状态又会反映在组织形态上,能否用 AI 学习二者之间的统计映射?于是,这项工作的目标被明确地限定为三点,不生成新的机制、不替代真实实验、只做一件事–把稀缺的免疫信息,扩展到可规模的人群,这一步,才是 GigaTIME 存在的意义。
训练数据:不是“拿公开数据随便训一训”论文中最重、也是最容易被忽略的工作,其实是数据工程。研究团队构建了一套严格配对的 H&E–mIF 数据集,同一块肿瘤组织、先进行 H&E 染色、再21通道多重免疫荧光染色、使用高精度图像配准算法,将两种染色对齐到同一空间坐标,随后,整张切片被切分为 256×256 像素的 patch,每个 patch 通常包含数百个细胞。在经历多轮质量控制(去背景、去配准失败区域、去低信息区域)后,最终用于训练的,是约5万个高质量配对patch,对应千万级细胞规模。这是一个非常昂贵、但不可替代的前置条件。
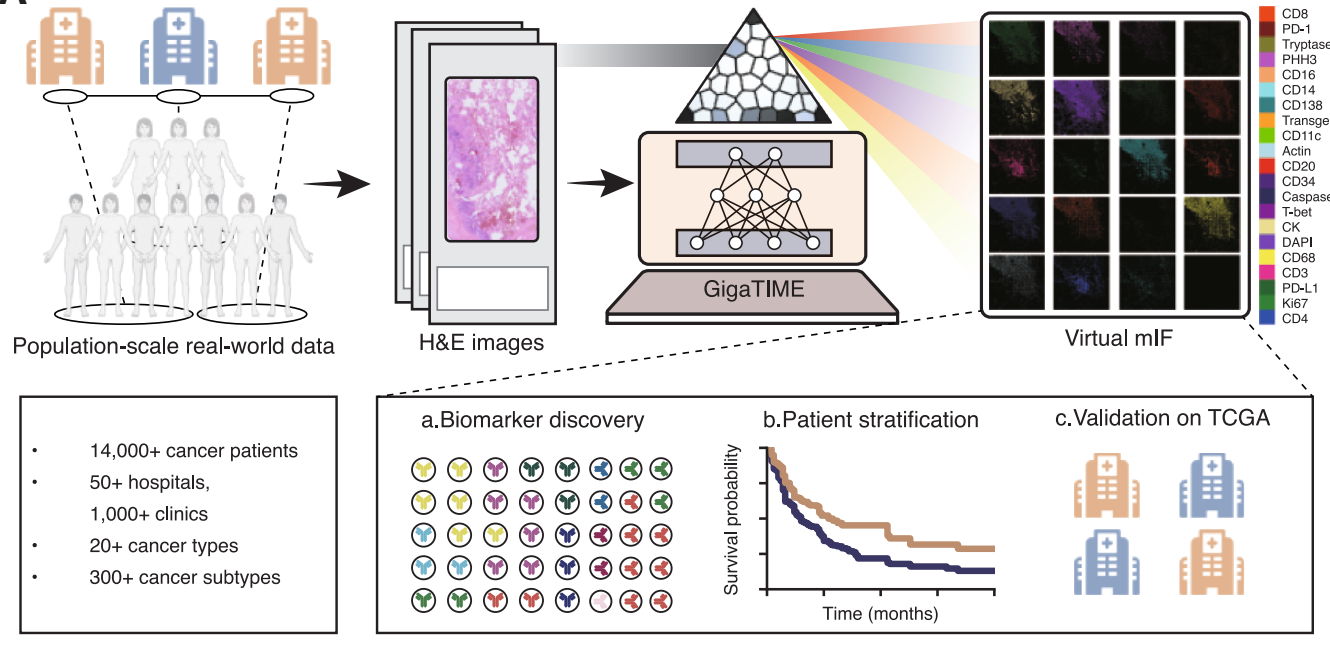
模型本身:并不炫技,但高度克制在模型选择上,微软团队的策略非常明确,稳定性优先于新颖性。最终使用的是 U-Net++(Nested U-Net),输入H&E patch,输出21 个免疫蛋白通道的空间激活图,每个通道被视为一个二值分割任务(激活 / 非激活),一个关键取舍是–连续荧光强度被二值化处理。这在表达精度上是妥协,但换来了三点好处,降低噪声、提高跨癌种泛化能力、让下游统计分析更稳健。
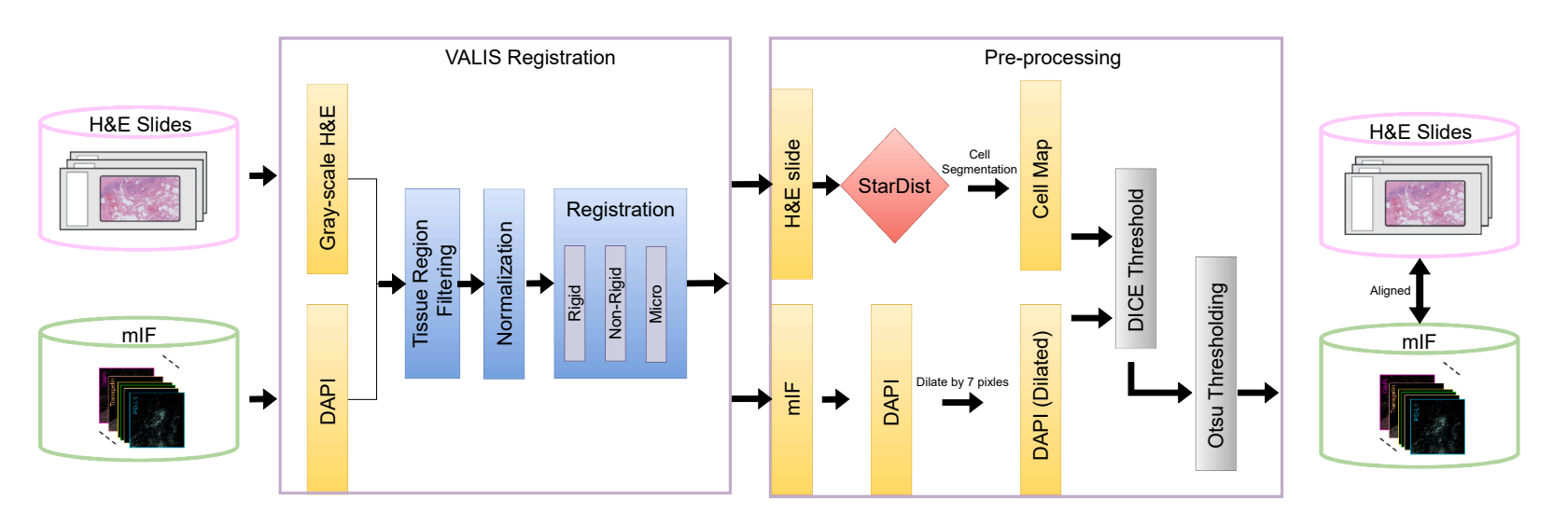
论文中也提到,他们测试过更大的 Vision Transformer,但计算成本极高,整体收益有限,并未作为最终方案。
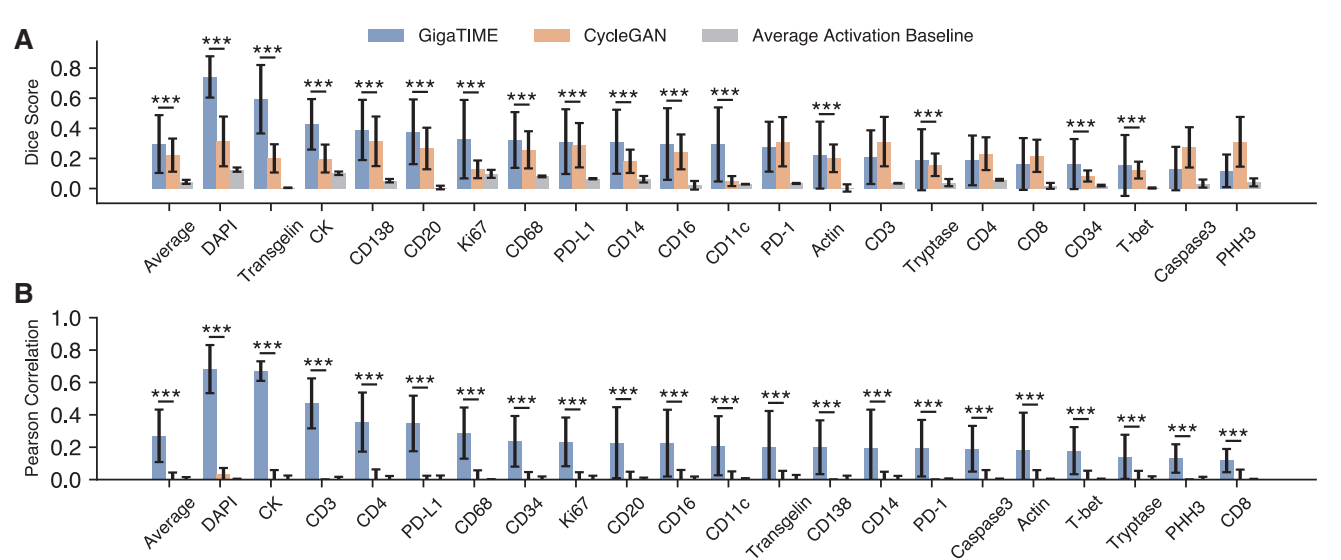
评估方式:不仅看“像不像”,还看“有没有统计意义”为了避免“AI 生成图像很好看,但没用”的问题,作者设计了三层评估体系:像素级,衡量预测的免疫蛋白空间位置是否准确(Dice 系数),细胞级,在局部窗口内统计激活像素,与真实 mIF 进行相关性比较(Pearson),空间结构级,在 patch 和 slide 层面评估免疫分布格局是否一致(Spearman),在所有层级上,GigaTIME 都显著优于 CycleGAN 等无监督方法。这一步的意义在于–它证明模型学到的不是“风格”,而是空间组织规律。
真正的高潮:虚拟免疫人群的构建模型训练完成后,真正的工作才开始。微软团队将 GigaTIME 应用到真实世界的 H&E 队列中,14,256 名患者、24 种癌症、300+ 组织学亚型、来自多州、多医疗系统,最终生成的是近 30 万张 21 通道的“虚拟免疫全切片”。
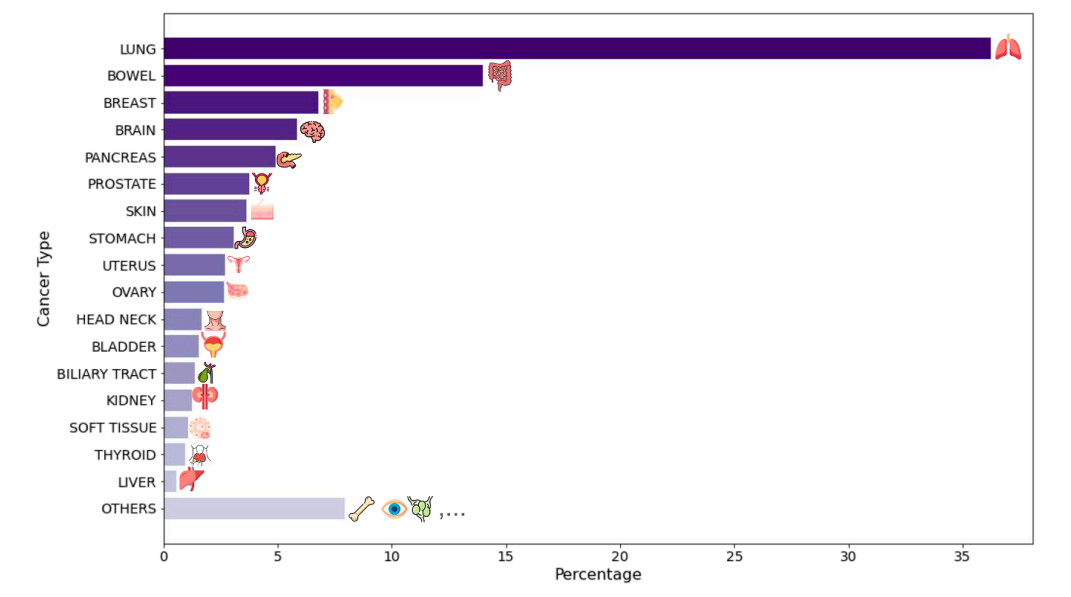
这些数据并不是展示用的,而是被当作一个真实可分析的人群,用于蛋白通道 × 临床生物标志物的系统关联分析、泛癌与亚型特异免疫模式比较、空间免疫结构指标(熵、信噪比、边缘复杂度)的统计研究。这一步,直接把空间免疫研究,推进到了类似基因组学的人群尺度。
它不是免疫学的终点这项工作并不意味着AI 取代实验、虚拟数据等于真实机制。它真正适合的角色是假说生成、人群分层、趋势发现,而因果验证,仍然必须回到真实实验。
【重要声明】以上内容仅用于知识科普,知识产权等所有权利归属于原作者,若有侵权,请联系esustain@163.com删除。
来源:CEll